Enfermedad de Chagas: de amenaza rural a problema de salud global
Foto de Public Health Image Library / CDC
Ideas clave
- La enfermedad de Chagas es curable pero menos del 1% de los afectados ha recibido tratamiento antiparasitario.
- La prevalencia mundial disminuyó un 55% entre 1990 y 2023, pero la migración está promoviendo la presencia de la enfermedad a regiones no endémicas.
- La transmisión congénita representa aproximadamente un tercio de las nuevas infecciones; el tratamiento en menores de un año tiene una tasa de éxito próxima al 100%.
- El 60-70% de los infectados permanece en forma indeterminada asintomática; el 30-40% restante desarrollará cardiopatía o formas digestivas graves en 10-30 años.
- Las vacunas candidatas basadas en antígenos de T. cruzi muestran resultados prometedores en modelos animales, con potencial para reducir la carga global de la enfermedad.
Introducción
La enfermedad de Chagas, descubierta en 1909 por el científico brasileño Carlos Ribeiro Justiniano Chagas, es una enfermedad infecciosa causada por el protozoo Trypanosoma cruzi. Progresa lentamente, a menudo de forma asintomática, y sin tratamiento puede provocar graves alteraciones cardíacas y digestivas e incluso la muerte. Es prevenible y curable, aunque menos del 10% de los afectados recibe diagnóstico y aproximadamente el 1% ha recibido tratamiento antiparasitario.
La enfermedad promueve y perpetúa la pobreza, afectando principalmente a personas vulnerables. Su coste sanitario se estima en 690 millones de dólares anuales, con pérdidas económicas anuales de 8.000 millones de dólares. Aproximadamente 75 millones de personas están en riesgo de contraerla.
Progreso epidemiológico
En 2023 se estimaron 10,5 millones de casos a nivel mundial, un 16,1% menos que en 1990. La prevalencia disminuyó un 55,0% y la mortalidad un 72,5% entre 1990 y 2023. La mayor prevalencia y mortalidad de la enfermedad ocurre en América Latina.
En 2023, se registraron 352.000 nuevos casos y 8.420 muertes. La distribución de la enfermedad se desplazó hacia edades más avanzadas. El pico de casos se situó entre los 45 y 65 años en 2023, frente a los 30-45 años de 1990. Las iniciativas de control vectorial han interrumpido la transmisión intradomiciliaria en 17 países, y se ha implementado el cribado universal de donantes de sangre en todos los países endémicos.
Las muertes por Chagas son frecuentemente subnotificadas —registradas como insuficiencia cardíaca o miocardiopatía inespecífica—, lo que dificulta conocer la carga real de la enfermedad. Las regiones no endémicas han experimentado aumentos de prevalencia debidos a la migración. Esto requiere nuevas estrategias de cribado y acceso a la atención.
Transmisión
La enfermedad se transmite por varias vías: vectorial (triatominos hematófagos), oral (alimentos contaminados), congénita (embarazo o parto), transfusional (sangre o productos sanguíneos), trasplante de órganos y accidentes de laboratorio. No se transmite a través de la leche materna.
La erradicación completa de la transmisión vectorial en América es imposible, por lo que la vigilancia de vectores debe ser continua. La transmisión oral es el principal mecanismo en la región amazónica. Se ha descrito brotes asociados al consumo de alimentos contaminados con triatominos o sus heces. La transmisión congénita afecta a alrededor de 1,12 millones de mujeres que están infectadas y en edad fértil. La tasa de transmisión congénita es de aproximadamente el 5%, con una incidencia de 8.000 a 15.000 casos anuales en América Latina.
La tasa de éxito del tratamiento antiparasitario en menores de 1 año es próxima al 100%. Respecto al trasplante de órganos, la donación de corazón e intestino está contraindicada en donantes infectados por el elevado riesgo de transmisión (75% o superior).

Presentación clínica
La infección evoluciona en dos fases. La fase aguda dura 4-8 semanas y, cuando es sintomática, cursa con fiebre persistente (más de 7 días), hepatoesplenomegalia, linfadenopatía, edema subcutáneo y exantema morbiliforme. El signo de Romaña —edema inflamatorio bipalpebral unilateral con hiperemia conjuntival y adenopatía preauricular— es un signo identificativo de la enfermedad. La fase aguda por transmisión oral tiende a ser más intensa, con algunos brotes de alta letalidad.
Entre el 60% y el 70% de los infectados nunca desarrollarán síntomas crónicos, manteniéndose en la forma indeterminada con pronóstico similar a la población no infectada.
El 30-40% restante evolucionará a formas sintomáticas al cabo de 10-30 años. Estas son la cardiopatía —la más prevalente, con tres grandes síndromes: muerte súbita, insuficiencia cardiaca y tromboembolismo— y formas digestivas (megaesófago o megacolon), predominantes en países al sur del Ecuador.
La enfermedad de Chagas congénita puede presentarse desde de forma asintomática hasta con fiebre, anemia, miocarditis o meningoencefalitis; el 28% de los lactantes infectados muestra síntomas clínicos y el 2,2% fallece.
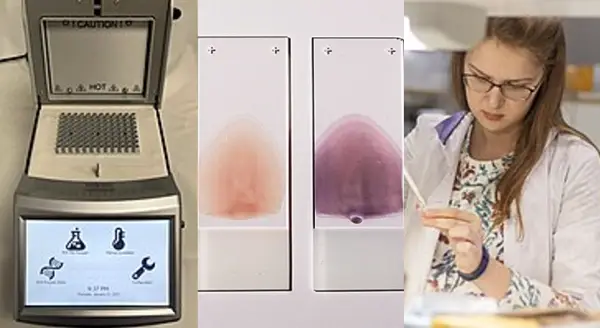
Avances en el diagnóstico
El diagnóstico crónico se basa en al menos dos pruebas serológicas con metodologías distintas (por ejemplo inmunoensayo enzimático e inmunoblot). Los resultados discordantes se resuelven con una tercera prueba, como la inmunofluorescencia.
Para distinguir la reactividad cruzada con la leishmaniasis puede estar indicada la realización de pruebas adicionales basadas por ejemplo en antígenos recombinantes.
En la fase aguda, el frotis en fresco permite detectar el parásito en sangre periférica, aunque requiere experiencia. Pasados 20-30 días pueden emplearse pruebas de concentración (microhematocrito o técnica de Strout). La PCR en tiempo real (rtPCR) cuantifica la carga parasitaria y resulta especialmente útil para el diagnóstico de la transmisión vertical y la detección precoz de reactivaciones en pacientes inmunosuprimidos.
Las pruebas de diagnóstico rápido, útiles como herramienta de cribado en el punto de atención, no deben emplearse como prueba única. Los resultados positivos deben confirmarse mediante serología convencional. La amplificación de tipo LAMP es otra técnica prometedora, más sencilla que la PCR y aplicable en recién nacidos e inmunosuprimidos.
El 70% de las personas infectadas desconoce su condición. El conocimiento sobre cribado y manejo entre los profesionales de la salud sigue siendo bajo tanto en países endémicos como no endémicos.
Tratamiento
La enfermedad de Chagas puede curarse con benznidazol o nifurtimox. Sin embargo, su eficacia disminuye cuanto más avanzada está la infección.
El tratamiento está indicado en la fase aguda, en la reactivación por inmunosupresión y al inicio de la fase crónica, especialmente en niñas y mujeres en edad fértil para prevenir la transmisión congénita. Ambos fármacos están contraindicados en embarazadas y en personas con insuficiencia renal o hepática. Además, el nifurtimox, no es adecuado en personas con antecedentes de trastornos neurológicos o psiquiátricos.
En la transmisión congénita, ambos fármacos son muy eficaces en el primer año de vida. En la fase crónica reciente (menos de 10 años de infección), la tasa de curación es de aproximadamente el 60%; con más de dos décadas de infección, se sitúa entre el 20% y el 40%.
El benznidazol no demostró reducir la mortalidad en la cardiopatía chagásica avanzada. En cuanto a tolerabilidad, los adultos presentan reacciones adversas con una frecuencia casi el doble que los niños. El nifurtimox se asocia a pérdida de peso y efectos psiquiátricos, y el benznidazol a reacciones cutáneas y neurológicas.
En estudios recientes se ha observado la capacidad de los amastigotes intracelulares para resistir el tratamiento. Por esto es necesario encontrar compuestos que eliminen estas formas del parásito. El tratamiento debe adoptar un enfoque integral: eliminación parasitaria, manejo de formas crónicas y apoyo psicosocial.
Desarrollo de vacunas
Se están estudiando varias vacunas. La vacuna basada en el antígeno Tc24-C4 ha demostrado reducir la inflamación cardíaca, la fibrosis y la carga parasitaria en modelos animales. Combinada con dosis bajas de benznidazol, mostró eficacia equivalente a dosis altas. Esta combinación, por tanto, tiene potencial para reducir la toxicidad del tratamiento.
También se ha observado que las vacunas de ARNm frente a los antígenos Tc24 y ASP-2 reducen la carga parasitaria y la inflamación cardíaca en ratones con enfermedad crónica.
Una tercera línea, basada en la familia de proteínas TcTASV mediante baculovirus recombinante, logró la supervivencia de más del 90% de los animales vacunados tras administrarles dosis letales de T. cruzi.
Las prioridades de investigación incluyen: nuevas moléculas antiparasitarias, formulaciones pediátricas, fármacos seguros para embarazadas, vacunas preventivas, y la identificación de un biomarcador de progresión de la enfermedad que permita orientar el tratamiento precoz y evitar la progresión a formas graves.
Estrategias de salud pública
Las estrategias clave de prevención incluyen: el control vectorial (en América Latina); el cribado de sangre antes de transfusiones y trasplantes, el cribado y tratamiento de niñas, mujeres en edad reproductiva y recién nacidos de madres infectadas, el diagnóstico precoz con seguimiento exhaustivo y la educación dirigida a comunidades y profesionales de la salud. El asesoramiento es fundamental para mejorar la adherencia y reducir el estigma.
La transmisión congénita representa aproximadamente un tercio de las nuevas infecciones, por lo que la detección precoz en embarazadas y recién nacidos es prioritaria.
El enfoque Una Salud es esencial para abordar retos emergentes como el cambio climático, la deforestación y la resistencia a insecticidas.
La hoja de ruta de la OMS para enfermedades tropicales desatendidas 2021-2030 incluye la meta de que 15 países eliminen la enfermedad de Chagas como problema de salud pública, interrumpiendo las cuatro vías de transmisión y alcanzando una cobertura del 75% con tratamiento antiparasitario.

Acciones clave
- Cribado universal de mujeres embarazadas en zonas endémicas y en contextos migratorios: la transmisión congénita representa un tercio de las nuevas infecciones, y el tratamiento en el primer año de vida tiene una tasa de éxito próxima al 100%, lo que convierte esta intervención en la de mayor retorno preventivo disponible.
- Incorporación de pruebas de diagnóstico rápido en atención primaria descentralizada: las pruebas de punto de atención no requieren laboratorio ni personal especializado y permiten aplicar el principio de diagnóstico y tratamiento inmediato, reduciendo la brecha entre los 10,5 millones de casos estimados y el 1% que actualmente recibe tratamiento.
- Implementación de la notificación obligatoria y la codificación correcta de muertes atribuibles a Chagas: la subnotificación sistemática —con muertes registradas como insuficiencia cardiaca inespecífica— oculta la carga real, impide políticas eficaces y bloquea la asignación de recursos; corregirla tiene coste bajo e impacto institucional y político elevado.
Si quieres saber más sobre enfermedades tropicales desatendidas no te pierdas este post sobre la cisticercosis.
Referencias
- Guide to Utilization of the Microbiology Laboratory for Diagnosis of Infectious Diseases: 2024 Update by the Infectious Diseases Society of America (IDSA) and the American Society for Microbiology (ASM). Clinical Infectious Diseases : An Official Publication of the Infectious Diseases Society of America. 2024. Miller JM, Binnicker MJ, Campbell S, et al. Guideline
- Neglected Parasitic Infections: What Family Physicians Need to Know—A CDC Update. American Family Physician. 2021. Cantey PT, Montgomery SP, Straily A.
- Chagas Cardiomyopathy: An Update of Current Clinical Knowledge and Management: A Scientific Statement From the American Heart Association. Circulation. 2018. Nunes MCP, Beaton A, Acquatella H, et al. Guideline
- Vaccine-Linked Chemotherapy Induces IL-17 Production and Reduces Cardiac Pathology During Acute Trypanosoma Cruzi Infection. Scientific Reports. 2021. Cruz-Chan JV, Villanueva-Lizama LE, Versteeg L, et al.
- Preclinical Advances and the Immunophysiology of a New Therapeutic Chagas Disease Vaccine. Expert Review of Vaccines. 2022. Jones KM, Poveda C, Versteeg L, Bottazzi ME, Hotez PJ.
- Harnessing RNA Technology to Advance Therapeutic Vaccine Antigens Against Chagas Disease. ACS Applied Materials & Interfaces. 2024. Mancino C, Pollet J, Zinger A, et al.
- Vaccination With Parasite-Specific TcTASV Proteins Combined With Recombinant Baculovirus as a Delivery Platform Protects Against Acute and Chronic Trypanosoma Cruzi Infection. Frontiers in Cellular and Infection Microbiology. 2023. Masip YE, Caeiro LD, Cosenza M, et al.
- Global, Regional, and National Burden of Chagas Disease, 1990-2023: A Systematic Analysis for the Global Burden of Disease Study 2023. The Lancet. Infectious Diseases. 2025. GBD 2023 Chagas Disease and RAISE Study Collaborators.
- Chagas Disease. Lancet. 2024. de Sousa AS, Vermeij D, Ramos AN, Luquetti AO.
- https://scientiasalut.gencat.cat/bitstream/handle/11351/3953/estoy_embarazada_tengo_chagas_2018_cas.pdf?sequence=5&isAllowed=y


