Malaria: logros y retos
Fotos de Jagamohan Senapati /Unsplash y Jimmy Chan / Pexels
Ideas clave
- Las mosquiteras tratadas con insecticida explican el 68% de la reducción de la malaria en África entre 2000 y 2022.
- Dos vacunas—RTS,S/AS01 y R21/Matrix-M— alcanzan hasta un 75% de eficacia con administración estacional, aunque su cobertura sigue limitada por financiación insuficiente.
- La resistencia parcial a la artemisinina, detectada en Camboya en 2007, se ha extendido a varios países africanos y amenaza los tratamientos de primera línea disponibles.
- Las mutaciones genéticas en parásitos de P. falciparum impiden su detección por pruebas rápidas en 42 países, con prevalencias superiores al 15% en seis de ellos.
- La malaria durante el embarazo mata a 10.000 mujeres africanas cada año y causa entre el 8% y el 14% de los nacimientos con bajo peso neonatal.
Introducción
La malaria es una enfermedad potencialmente letal que se transmite por la picadura de hembras infectadas de mosquitos del género Anopheles. Ocurre sobre todo en países tropicales. La infección está causada por un parásito y no se transmite de persona a persona. Es una enfermedad prevenible y curable. De no tratarse, la malaria por P. falciparum puede causar la muerte en 24 horas. Según un artículo de la OPS la maria mata a un niño cada 2 minutos.
Carga global
En 2024 se produjeron 282 millones de casos y 610.000 muertes en 80 países. África concentró el 95% de los casos y el 95% de las muertes, de las cuales alrededor del 75% correspondió a niños menores de 5 años. Más de la mitad de todas las muertes en África se produjeron en tres países: Nigeria (31,9%), la República Democrática del Congo (11,7%) y el Níger (6,1%).
Entre 2000 y 2022 se registró una reducción del 40% en la incidencia y del 60% en la mortalidad en África. El 68% de esta reducción se asoció al uso de mosquiteras tratadas con insecticida, el 22% a los programas de terapias combinadas con artemisinina y el 10% al rociado residual en interiores.

Síntomas y poblaciones de riesgo
Los síntomas leves incluyen fiebre, escalofríos y dolor de cabeza. Los graves comprenden fatiga, confusión, convulsiones y dificultad para respirar. Los síntomas suelen aparecer a los 10-15 días de la picadura. Entre los síntomas graves adicionales figuran orina oscura o con sangre, coloración amarillenta de ojos y piel, y hemorragias anormales.
Las poblaciones con mayor riesgo son lactantes, menores de 5 años, mujeres embarazadas, viajeros y personas con VIH o sida.
La infección durante el embarazo puede causar parto prematuro o bajo peso al nacer. Las mujeres embarazadas tienen tres veces más riesgo de infección que las no embarazadas. La malaria en el África subsahariana mata a 10.000 mujeres embarazadas cada año y causa entre el 8% y el 14% de los recién nacidos con bajo peso y entre el 3% y el 8% de las muertes neonatales.
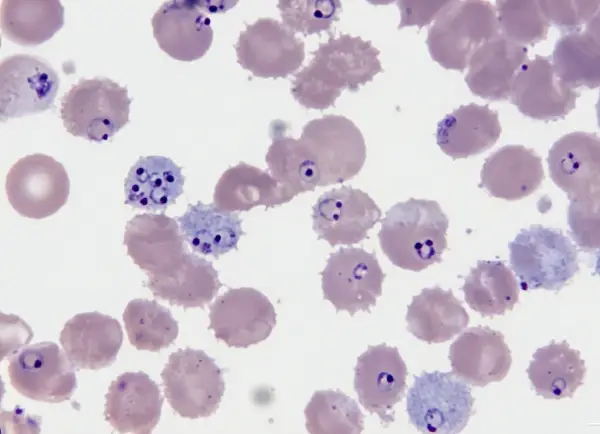
Parásitos causantes
Cinco especies de Plasmodium pueden provocar malaria en humanos. P. falciparum es el más mortífero y prevalente en África, responsable de más del 90% de la mortalidad mundial por malaria. P. vivax es dominante en varios países fuera del África subsahariana. Las otras especies son P. malariae, P. ovale y P. knowlesi.
P. falciparum y P. vivax constituyen la mayor amenaza global. P. falciparum causa la mayoría de las muertes y P. vivax es la especie de malaria más extendida a nivel mundial. Puede causar infecciones graves, incluso mortales. P. malariae se encuentra en Suramérica, Asia y África. Solo invade eritrocitos envejecidos y tiene poca incidencia. P. ovale se localiza en África y países del Pacífico Occidental. P. knowlesi se ha detectado en el Sudeste Asiático, y las personas que trabajan en el bosque son la que corren mayor riesgo de infección. Casi no hay presencia de P. knowlesi en África.
Prevención y control vectorial
La malaria puede prevenirse evitando las picaduras de mosquitos y curarse con medicamentos. Las dos principales intervenciones de control vectorial son las mosquiteras tratadas con insecticida y el rociado de interiores con insecticidas de acción residual. Se ha observado que las mosquiteras reducen la mortalidad infantil en un 17%, la prevalencia parasitaria en un 13%, los episodios de malaria no complicada en un 50% y la malaria grave en un 45%.
El rociado residual en interiores redujo el riesgo de malaria en un 65%. Sin embargo, la creciente resistencia a los insecticidas reduce la eficacia de ambas intervenciones. La especie invasora Anopheles stephensi, originaria de Asia Meridional, se ha extendido a ocho países africanos en la última década. Prospera en entornos urbanos y es resistente a muchos insecticidas.
Los medicamentos para prevenir la malaria estacional durante las temporadas de alta transmisión han logrado reducir la morbilidad y mortalidad. Principalmente en niños en edad preescolar en el África subsahariana. Los medicamentos para prevenir la malaria perenne reducen la incidencia clínica, las hospitalizaciones y la anemia en niños menores de 2 años.
Vacunas
Dos vacunas preeritrocíticas dirigidas contra Plasmodium falciparum han recibido el respaldo de la OMS: RTS,S/AS01 recomendada por la OMS en 2021 y R21/Matrix-M recomendada por la OMS en 2023. Ambas actúan sobre la misma proteína de superficie del parásito y la pauta de vacunación consiste en varias dosis.
En un ensayo, RTS,S/AS01redujo la malaria clínica en un 36% en niños de 5 a 17 meses y en un 26% en lactantes de 3 a 4 meses. Su implementación en Ghana, Kenia y Malawi demostró una reducción del 32% en los ingresos hospitalarios por malaria grave y del 9% en las muertes infantiles.
Además, RTS,S/AS01 redujo los casos de malaria en un 51% durante el año posterior a la vacunación, y en un 72% con vacunación estacional. La protección disminuye con el tiempo.
En el caso de la vacuna R21/Matrix-M, los ensayos demostraron una eficacia del 75% en centros de vacunación estacionales y del 68% en centros estándar durante 12 meses. Redujo la malaria clínica en un 66% en los 12 meses siguientes a la vacunación.
Los estudios han demostrado que administrar las tres primeras dosis de la vacuna antes de la temporada de lluvias (administración estacional) mejora la eficacia de ambas vacunas. Ambas vacunas reducen los casos en aproximadamente un 75% cuando se administran estacionalmente en zonas de alta transmisión estacional. Sin embargo, la administración estacional es mucho más difícil de implementar que la administración basada en la edad. Este segundo enfoque consiste en administrar tres dosis de la vacuna a partir de los 5 meses de edad, y una cuarta dosis alrededor de los 2 años para prolongar la protección.
No hay evidencia de que una vacuna sea mejor que la otra.
Actualmente 25 países africanos ofrecen estas vacunas en sus programas de vacunación infantil, con el objetivo de vacunar a más de 10 millones de niños anualmente. Las limitaciones de financiación impiden alcanzar los objetivos nacionales en muchos países. Si se lograra una cobertura vacunal del 100%, se estima que se podrían prevenir hasta 10 millones de casos y 51.000 muertes de menores de 5 años cada año.
Diagnóstico
Los principales métodos diagnósticos son la microscopía de frotis de sangre periférica, las pruebas de diagnóstico rápido, la PCR y los biomarcadores emergentes. La microscopía es el estándar de referencia recomendado por la OMS, pero la calidad de los resultados depende de la pericia del microscopista. Las pruebas de diagnóstico rápido presentan una sensibilidad del 92% y una especificidad del 96,6% para P. falciparum. La PCR alcanza una especificidad y sensibilidad de hasta el 88-100%, pero requiere equipamiento especializado que no es posible desplegar de forma masiva en países con escasos recursos.
En 2024 se notificó por primera vez la presencia de parásitos con mutaciones genéticas que impiden su detección por pruebas de diagnóstico rápido en 42 países, con prevalencia superior al 15% en Brasil, Djibouti, Eritrea, Etiopía, Nicaragua y Perú.
Los biomarcadores representan una tecnología emergente con alta sensibilidad para uso en puntos de atención en zonas de recursos limitados.
Tratamiento
La toma de varios fármacos a base de artemisinina es el tratamiento más eficaz contra P. falciparum no grave. Para la malaria grave, el artesunato intravenoso es el tratamiento de primera elección; comparado con la quinina, reduce la mortalidad en niños africanos en un 22,5%. La cloroquina está recomendada para P. vivax solo en zonas donde aún es sensible al fármaco. La primaquina previene recaídas de P. vivax y P. ovale y debe añadirse al tratamiento principal.
Resistencia a los medicamentos
La resistencia parcial a la artemisinina, confirmada por primera vez en Camboya en 2007, se encuentra actualmente extendida en el sudeste asiático y África. La OMS ha confirmado resistencia en Eritrea, Tanzania, Rwanda y Uganda, y la sospecha en Etiopía, Namibia, Sudán y Zambia.
Se ha demostrado que la alternancia de fármacos podría reducir la resistencia. Las terapias combinadas triples, que combinan una artemisinina con dos fármacos asociados ya existentes, podrían ser uno de los últimos tratamientos seguros y eficaces contra P. falciparum multirresistente.
Las mutaciones en el gen Kelch13 (K13) son el principal marcador de la resistencia a la artemisinina.
Eliminación
En 2024, 37 países notificaron menos de 1.000 casos autóctonos. Desde 2015, la OMS ha certificado la ausencia de malaria en 17 países, incluyendo Georgia, Suriname y Timor-Leste en 2025. La Estrategia Técnica Mundial 2016-2030 establece como metas reducir la incidencia y la mortalidad en al menos un 90% y eliminar la enfermedad en al menos 35 países para 2030.
Líneas de investigación prioritarias
Las áreas prioritarias incluyen el desarrollo de nuevos fármacos esquizonticidas sanguíneos activos contra parásitos resistentes a la artemisinina, regímenes simplificados de primaquina para la cura de P. vivax, nuevos fármacos hipnozoiticidas, vacunas preeritrocíticas mejoradas, vacunas que bloqueen la transmisión, vacunas contra P. vivax y métodos de diagnóstico rápido para los parásitos resistentes a los medicamentos y para detectar la deficiencia de G6PD.
La deficiencia de G6PD es una enfermedad hereditaria resultante de un defecto en la enzima G6PD. Existe un solapamiento entre la prevalencia de la deficiencia de G6PD y la de P. vivax. El fármaco para tratar la malaria por Plasmodium vivax es la primaquina. Aunque es eficaz, en pacientes con deficiencia de la enzima G6PD puede desencadenar un trastorno sanguíneo grave conocido como anemia hemolítica aguda.
Tres acciones
- Ampliar la vacunación estacional con RTS,S/AS01 o R21/Matrix-M antes de la temporada de lluvias en zonas de alta transmisión estacional podría reducir los episodios de malaria hasta en un 75%, con un impacto potencial de 51.000 muertes infantiles evitadas anualmente a cobertura completa.
- Reforzar la vigilancia de mutaciones en pfhrp2/pfhrp3 en los 42 países con parásitos indetectables por pruebas rápidas estándar, sustituyendo o complementando estas pruebas con PCR o microscopía, evitaría un infradiagnóstico que compromete el tratamiento oportuno y la vigilancia epidemiológica.
- Distribuir mosquiteras tratadas con insecticida en poblaciones no cubiertas, especialmente embarazadas y menores de cinco años, podría generar reducciones del 50% en episodios de malaria no complicada y del 45% en malaria grave, con una relación coste-impacto demostrada como la más favorable de todas las intervenciones disponibles.

Referencias
- Malaria. Lancet. 2023. Poespoprodjo JR, Douglas NM, Ansong D, Kho S, Anstey NM.
- Diagnosis, Treatment, and Prevention of Malaria in the US: A Review. The Journal of the American Medical Association. 2022. Daily JP, Minuti A, Khan N.
- Feasibility, Safety, and Impact of the RTS,S/AS01E Malaria Vaccine When Implemented Through National Immunisation Programmes: Evaluation of Cluster-Randomised Introduction of the Vaccine in Ghana, Kenya, and Malawi. Lancet. 2024. Asante KP, Mathanga DP, Milligan P, et al.
- Safety and Efficacy of Malaria Vaccine Candidate R21/Matrix-M in African Children: A Multicentre, Double-Blind, Randomised, Phase 3 Trial. Lancet. 2024. Datoo MS, Dicko A, Tinto H, et al.
- Evolution and Expansion of Multidrug-Resistant Malaria in Southeast Asia: A Genomic Epidemiology Study. The Lancet. Infectious Diseases. 2019. Hamilton WL, Amato R, van der Pluijm RW, et al.
- Malaria. The New England Journal of Medicine. 2025. Daily JP, Parikh S.
- Changes in Susceptibility of Plasmodium Falciparum to Antimalarial Drugs in Uganda Over Time: 2019-2024. Nature Communications. 2025. Okitwi M, Orena S, Tumwebaze PK, et al.
- Plasmodium vivax Malaria. [Updated 2023 Jul 17]. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2026 Jan-.Disponible en https://www.ncbi.nlm.nih.gov/books/NBK538333/ Menkin-Smith L, Winders WT
- Current Status of Malaria Control and Elimination in Africa: Epidemiology, Diagnosis, Treatment, Progress and Challenges. J Epidemiol Glob Health. 2024 Sep;14(3):561-579. doi: 10.1007/s44197-024-00228-2. Epub 2024 Apr 24. PMID: 38656731; PMCID: PMC11442732. Li J, Docile HJ, Fisher D, Pronyuk K, Zhao L.
- https://www.who.int/es/news-room/questions-and-answers/item/q-a-on-rts-s-malaria-vaccine
- https://www.gavi.org/vaccineswork/how-effective-are-malaria-vaccines
- https://www.who.int/es/news-room/fact-sheets/detail/malaria
- https://www.who.int/teams/global-malaria-programme/case-management/diagnosis/rapid-diagnostic-tests/g6pd-rapid-diagnostic-tests
- https://www.paho.org/es/historias/destino-eliminacion-malaria-choco-epicentro-esta-enfermedad-por-plasmodium-falciparum


